Η πρώτη γονιδιακή θεραπεία με βάση τη βραβευμένη με Νόμπελ τεχνική CRISPR, σχεδιάστηκε για σπάνιες κληρονομικές αιματολογικές νόσους και θα κυκλοφορήσει στην αγορά έως το 2023, ανοίγοντας δρόμο για μελλοντική ανάπτυξη τέτοιων θεραπειών. Ωστόσο, παραμένει ανοικτό το ερώτημα αν αυτές θα είναι για όλους.
Μέχρι πρόσφατα, το CRISPR/Cas9, η τεχνολογία επεξεργασίας γονιδίων που χάρισε στις Jennifer Doudna και Emmanuelle Charpentier το Νόμπελ Χημείας 2020, ακουγόταν περισσότερο σαν επιστημονική φαντασία και λιγότερο ως ιατρική τεχνική. Ωστόσο, το «μοριακό ψαλίδι» που δημιουργήθηκε στο εργαστήριο για να επιδιορθώνει προβληματικά τμήματα DNA στα ανθρώπινα κύτταρα προκειμένου να θεραπευθεί μια ασθένεια, σύντομα θα μπορεί να εγκριθεί από τις ρυθμιστικές αρχές ως η πρώτη θεραπεία καταπολέμησης σπάνιων κληρονομικών αιματολογικών διαταραχών που επηρεάζουν εκατομμύρια ανθρώπους παγκοσμίως.
Η συνεργασία των 900 $ εκατομμυρίων της εξειδικευμένης σε σπάνιες νόσους αμερικανικής φαρμακευτικής Vertex με την ελβετο-αμερικανική εταιρεία βιοτεχνολογίας CRISPR Therapeutics απέφερε την exa-cel (exagamglogene autotemcel), μια πολλά υποσχόμενη θεραπεία για ασθενείς με β-θαλασσαιμία και δρεπανοκυτταρική αναιμία, που είναι γενετικές διαταραχές του αίματος.
Αυτή τη στιγμή «τρέχουν» δυο δοκιμές Φάσης ΙΙΙ (οι CLIMB-141 και CLIMB-151) για την ασφάλεια και την αποτελεσματικότητα μιας εφάπαξ δόσης exa-cel σε ασθενείς ηλικίας 2-11 ετών με β-θαλασσαιμία και δρεπανοκυτταρική αναιμία αντίστοιχα, οι οποίοι παρακολουθούνται για μια 2ετία περίπου μετά την έγχυση. Σε επόμενο στάδιο, κάθε ασθενής θα κληθεί να συμμετάσχει σε μια μακροχρόνια δοκιμή παρακολούθησης, στην CLIMB-131.
Οι παραγωγοί της θεραπείας σκοπεύουν να καταθέσουν αίτηση στις ρυθμιστικές αρχές των ΗΠΑ, του Ην. Βασιλείου και της Ευρώπης για έγκριση της exa-cel μέχρι το τέλος του τρέχοντος έτους, πράγμα που σημαίνει ότι το φάρμακο θα λάβει άδεια κυκλοφορίας κάποια στιγμή μέσα στο 2023.
Θεραπευτικά προϊόντα προηγμένης τεχνολογίας
Τα προϊόντα γονιδιακής θεραπείας, όπως η exa-cel συνιστούν τη 1 από τις 3 ετερογενείς κατηγορίες σύγχρονων θεραπευτικών και φαρμακευτικών προϊόντων που βασίζονται σε τεχνολογίες αιχμής και που προσφέρουν θεραπεία εφάπαξ.
«Πρόκειται για τα επονομαζόμενα Advanced Therapeutic Medicinal Products (ATMPs), τα οποία, σύμφωνα με τον Ευρωπαϊκό Οργανισμό έγκρισης θεραπευτικών προϊόντων (EMA), προορίζονται για ανθρώπινη χρήση και βασίζονται σε γονίδια, ιστούς ή κύτταρα. Οι άλλες δυο κατηγορίες περιλαμβάνουν τα προϊόντα σωματοκυτταρικής θεραπείας και τα προϊόντα μηχανικής των ιστών. Εκτός από αυτές υπάρχει και μια τέταρτη κατηγορία, που περιλαμβάνει τα ιατροτεχνολογικά προϊόντα, γνωστά ως complementary ATMPs'», εξηγεί ο Κωνσταντίνος Δεμέτζος, που είναι Καθηγητής Φαρμακευτικής Νανοτεχνολογίας, Διευθυντής του Εργαστηρίου της Φαρμακευτικής Τεχνολογίας, ΕΚΠΑ και Τακτικό μέλος της Ευρωπαϊκής Ακαδημίας Επιστημών και Τεχνών, διευκρινίζοντας πως τα γονιδιακά θεραπευτικά προϊόντα που στηρίζονται σε ανασυνδυασμένα γονίδια με στόχο την προφύλαξη, τη διάγνωση ή την θεραπεία ασθενειών, χρησιμοποιούνται σε γενετικές διαταραχές, σε αντίθεση με θεραπείες με σωματικά κύτταρα που χρησιμοποιούν βιολογικά επεξεργασμένα κύτταρα ή ιστούς ή με προϊόντα μηχανικής των ιστών που περιέχουν τροποποιημένα κύτταρα ή ιστούς για να "επισκευάσουν", αναγεννήσουν ή αντικαταστήσουν ανθρώπινο ιστό. Τα βλαστοκύτταρα αποτελούν επίσης αναπόσπαστο τμήμα των ATMPs καθώς αποτελούν συστατικά θεραπειών με σωματικά κύτταρα που παράγονται από ιστούς.

Ο Καθηγητής Φαρμακευτικής Νανοτεχνολογίας, Διευθυντής του Εργαστηρίου της Φαρμακευτικής Τεχνολογίας, ΕΚΠΑ και Τακτικό μέλος της Ευρωπαϊκής Ακαδημίας Επιστημών και Τεχνών, Κ.Δεμέτζος
Στην Ευρώπη και στις ΗΠΑ, τα ATMPs θεωρούνται βιολογικά προϊόντα αναφορικά με το ρυθμιστικό τους πλαίσιο. Αυτή τη στιγμή, υπάρχουν περίπου 20 κυτταρικές και γονιδιακές θεραπείες (αν και καμία δεν βασίζεται στην επεξεργασία γονιδίων CRISPR/Cas9) που έχουν λάβει έγκριση από τον FDA. Σύμφωνα με το πρόγραμμα ανάπτυξης φαρμάκων NEWDIGS του MIT, περισσότερες από 60 γονιδιακές και κυτταρικές θεραπείες θα μπορούσαν να κυκλοφορήσουν στην αγορά των ΗΠΑ έως το 2030.
Ενθαρρυντικά τα κλινικά δεδομένα της exa-cel
Η β-θαλασσαιμία χαρακτηρίζεται από κατεστραμμένα ή ελλιπή γονίδια που οδηγούν σε ανεπάρκεια αιμοσφαιρίνης για τη μεταφορά οξυγόνου. Υπολογίζεται ότι η διαταραχή ταλαιπωρεί 1 στους 100.000 ανθρώπους παγκοσμίως, αναγκάζοντάς τους να υποβάλλονται σε τακτικές μεταγγίσεις αίματος για να αποφεύγουν πιο σοβαρές επιπτώσεις της. Αντίστοιχα η δρεπανοκυτταρική αναιμία που επηρεάζει 6 εκατομμύρια ανθρώπους σε όλο τον κόσμο, αποδίδεται σε ένα ελαττωματικό γονίδιο αιμοσφαιρίνης που προκαλεί δυσμορφία στα ερυθροκύτταρα (δρεπανοειδή μορφή), η οποία δυσκολεύει τη μεταφορά οξυγόνου στους ιστούς.
Η exa-cel έδειξε να μειώνει την ανάγκη για μεταγγίσεις αίματος ή τη συχνότητα εμφάνισης σοβαρών, απειλητικών για τη ζωή περιστατικών για μήνες έως χρόνια αφότου οι ασθενείς έλαβαν τη θεραπεία. Τα εντυπωσιακά αποτελέσματα των κλινικών δοκιμών που ανακοινώθηκαν πέρσι στο διεθνές ιατρικό συνέδριο της European Hematology Association, (EHA) στην Ελβετία ενίσχυσαν την προοπτική παραγωγής της πρώτης θεραπεία με γονιδιακή επεξεργασία CRISPR/Cas9 που θα φτάσει σύντομα στην ευρύτερη αγορά και στους ασθενείς.
Η παραγωγή της θεραπείας στηρίζεται στην "ex-vivo" (εκτός σώματος) εφαρμογή της γονιδιακής επεξεργασίας CRISPR/Cas9.Τα βλαστοκύτταρα του ασθενούς εξάγονται, για να τροποποιηθεί το γενετικό τους υλικό από την ex-cel και να τονωθεί η παραγωγή ένας τύπου αιμοσφαιρίνης που το σώμα παράγει μόνο στη βρεφική ηλικία. Στη συνέχεια, τα τροποποιημένα κύτταρα επανατοποθετούνται στον ασθενή προκειμένου να ενισχυθεί η υγιής αιμοσφαιρίνη και η παραγωγή ερυθρών αιμοσφαιρίων.
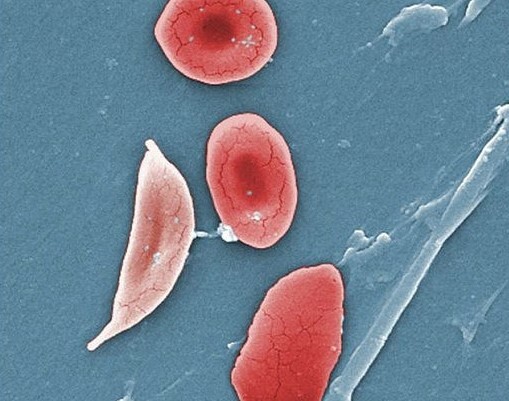
wikimedia commons
Τα τελευταία κλινικά δεδομένα που παρουσιάστηκαν στην Ελβετία, έδειξαν ότι όλοι οι ασθενείς με β-θαλασσαιμία ή δρεπανοκυτταρική νόσο (75 συνολικά) που έλαβαν την ex-cel παρουσίασαν μηδενική ή πολύ μειωμένη ανάγκη μετάγγισης αίματος. Οι 42 εκ των 44 ασθενών με β-θαλασσαιμία δεν χρειάστηκαν ούτε μία μετάγγιση για 1 έως 37 μήνες μετά τη χορήγηση της θεραπείας, ενώ οι υπόλοιποι 2 χρειάστηκαν κατά 75% και 89% λιγότερη ποσότητα αίματος κατά τη μετάγγιση.
Παρομοίως όλοι οι ασθενείς (31 συνολικά) με σοβαρή και απειλητική για τη ζωή μορφή δρεπανοκυτταρικής δεν παρουσίασαν αγγειοαποφρακτικές κρίσεις για 2 έως 32 μήνες μετά τη θεραπεία. Οι ίδιοι, δυο χρόνια πριν λάβουν τη θεραπεία βίωναν κατά μέσο όρο, σχεδόν τέσσερα τέτοια περιστατικά ετησίως.
Η γονιδιακή επεξεργασία δεν είναι αθώα
«Προτεραιότητα στην ανάπτυξη θεραπευτικών προϊόντων προχωρημένης τεχνολογίας (ATMPs) έχουν οι γενετικές, κυτταρικές και χρόνιες φλεγμονώδεις παθήσεις όπως η ανοσοανεπάρκεια και ο καρκίνος. Από το 2016 «τρέχει» το 85% χιλίων περίπου κλινικών δοκιμών σε ATMPs, η πλειονότητα των οποίων βρίσκεται σε κλινική φάση Ι ή ΙΙ. Από τις κλινικές αυτές δοκιμές το 54% αφορά θεραπείες με σωματικά κύτταρα, το 23% προϊόντα μηχανικής των ιστών και το 22% γονιδιακές θεραπείες, ενώ περίπου το 1% αφορά σε συνδυασμό προϊόντων. Ο κύριος τομέας εφαρμογής των ATMPs είναι ο καρκίνος, τα καρδιοαγγειακά προβλήματα και ασθένειες του ανοσοποιητικού συστήματος και φλεγμονές», παρεμβαίνει ο Καθ. Δεμέτζος.
Σύμφωνα με τον ίδιο, η γονιδιακή επεξεργασία CRISPR/Cas9 δεν είναι ο μόνος τύπος γονιδιακής θεραπείας που δημιούργησε θόρυβο. Νωρίτερα, μια ομάδα συμβούλων του FDA έδωσε ομόφωνες συστάσεις για ένα ζευγάρι γονιδιακών θεραπειών της εταιρείας Bluebird Bio που δεν βασίζονται στη CRISPR/Cas9. Οι θεραπείες στοχεύουν γονίδια που σχετίζονται με τη β-θαλασσαιμία και με μια σπάνια διαταραχή, την εγκεφαλική αδρενολευκοδυστροφία (CALD) που κατατρώει τη λευκή ουσία του εγκεφάλου παιδιών ηλικίας 4 ετών και που συνήθως οδηγεί σε θάνατο μέσα σε 5-10 χρόνια. Ωστόσο, οι κλινικές δοκιμές αυτής της θεραπείας απέτυχαν λόγω της συσχέτισής της με υψηλό κίνδυνο εμφάνισης ενός τύπου καρκίνου, παρότι οι ανεξάρτητοι σύμβουλοι έκριναν ότι τα οφέλη της εξακολουθούν να υπερτερούν των κινδύνων για ορισμένους ασθενείς με περιορισμένες εναλλακτικές.
«Δυστυχώς πολλές γονιδιακές θεραπείες συχνά συνοδεύονται από επικίνδυνες παρενέργειες. Δεν είναι τυχαίο το γεγονός ότι από τις 10 γονιδιακές θεραπείες που εγκρίθηκαν στο χρονικό διάστημα 2009-2018, οι 4 αποσύρθηκαν λόγω σοβαρών παρενεργειών», συμπληρώνει ο Καθ. Δεμέτζος
Δεν είναι εύκολη η έγκριση
Σύμφωνα με τον Έλληνα επιστήμονα, οικονομικά, δεοντολογικά και ρυθμιστικά είναι τα ζητήματα που σχετίζονται με τα θεραπευτικά προϊόντα προηγμένης τεχνολογίας (ATMPs): «Τα ATMPs αντιμετωπίζονται διαφορετικά από τις συμβατικές θεραπείες όσον αφορά στην ανάπτυξη και στην παραγωγή τους. Ένας κρίσιμος παράγοντας είναι η μεταβλητότητα από παρτίδα σε παρτίδα κατά την παραγωγή τους εξαιτίας της πολυπλοκότητας τους. Η τυποποίηση των διαδικασιών παραγωγής και η θέσπιση καλών προτύπων παραγωγής, πολύπλοκων κλινικών μελετών, ετερογένειας στις κανονιστικές και ρυθμιστικές αρχές καθώς και ζητημάτων αποζημίωσης, δημιουργούν ένα πολύπλοκο σύστημα και ένα πολυπαραγοντικό πεδίο διαχείρισης», τονίζει ο ίδιος.
Είναι ενδιαφέρον ότι οι κλινικές δοκιμές μέχρι πρότινος δεν περιλάμβαναν περισσότερους από 25 εθελοντές και σύμφωνα με μελέτες περίπτωσης οι περισσότερες αρνητικές αξιολογήσεις των ATMPs αποδίδονται σε έλλειψη επαρκών κλινικών μελετών. Ωστόσο, οι ανάγκες για θεραπεία συχνά λειτουργούν εξισορροπητικά για την έγκριση τους.
«Είναι προφανές ότι υπάρχει ανάγκη επαρκούς ρυθμιστικού πλαισίου αξιολόγησης. Τα ATMPs σήμερα αδειοδοτούνται εντός της ΕΕ μέσω μια κεντρικής διαδικασίας αξιολόγησης, ενώ ο τομέας της βιοηθικής αποτελεί αντικείμενο συζήτησης. Τον κανονισμό έγκρισης διαχειρίζεται η Επιτροπή προηγμένων θεραπειών (Committee of Advanced Therpies, CAT), ενώ έχουν επίσης αναπτυχθεί ειδικές ρυθμιστικές οδοί, συμπεριλαμβανομένου και του Προγράμματος Φαρμάκων Προτεραιότητας (PRIME), για την ταχεία αξιολόγηση και έγκριση υπό όρους και της παρηγορητικής χρήσης αυτών. Τέλος δεδομένου ότι τα θεραπευτικά αυτά προϊόντα προορίζονται για σπάνιες νόσους χαρακτηρίζονται ως "ορφανά"», καταλήγει ο Έλληνας επιστήμονας
Γονιδιακές θεραπείες για όλους
Η διαθεσιμότητα περισσότερων γονιδιακών θεραπειών θα επιφέρει βαθιές τομές στο πεδίο της αντιμετώπισης πολλών σπάνιων γενετικών ασθενειών. Τα συστήματα υγειονομικής περίθαλψης παγκοσμίως καλούνται τώρα να διασφαλίσουν ότι όλοι οι ασθενείς και όχι μόνο οι εκλεκτοί με οικονομικά μέσα και προνομιακή πρόσβαση στην τεχνολογία, θα μπορούν να επωφεληθούν από αυτές τις καινοτόμες θεραπείες.
Η δρεπανοκυτταρική αναιμία επηρεάζει συντριπτικά την Αφρική. Περίπου το 90% των παιδιών που γεννιούνται με αυτήν μπορεί να πεθάνουν πριν από τα πέντε τους χρόνια. Οι ειδικοί πιστεύουν ότι τα προϊόντα γονιδιακής θεραπείας της νόσου θα αγγίξουν πιθανώς τα 2 εκατομμύρια δολάρια για μια εφάπαξ δόση! Χωρίς πρόσβαση στην υγειονομική περίθαλψη, 9 στα 10 παιδιά με τη νόσο στις χώρες χαμηλού και μεσαίου εισοδήματος αγωνίζονται να γιορτάσουν τα 5α γενέθλιά τους.
Παρότι οι τιμές των φαρμάκων υπόκεινται στους ρυθμιστικούς κανονισμούς των χωρών, η τιμολόγηση των γονιδιακών θεραπειών παραμένει σε μεγάλο βαθμό ανεξέλεγκτη και αποφασίζεται κατά περίπτωση. Στον καθορισμό της τιμής, οι παραγωγοί τους περιλαμβάνουν το κόστος ανάπτυξης, τα ειδικά χαρακτηριστικά της νόσου τις σχετικές δαπάνες, αλλά και τις νοσηλείες και τη χαμένη παραγωγικότητα, που μπορούν δυνητικά να αποφευχθούν με τη θεραπεία. Οι τιμές επηρεάζονται επίσης και από την έλλειψη ανταγωνισμού, αφού είναι λίγες οι εταιρείες που αναπτύσσουν γονιδιακές θεραπείες για σπάνιες ασθένειες, οι οποίες απευθύνονται επίσης σε έναν περιορισμένο αριθμό ασθενών. Άρα τα κέρδη από έναν μικρό αριθμό δόσεων πρέπει να αντισταθμίσουν ολόκληρο το κόστος ανάπτυξης και παραγωγής της θεραπείας.
Οι ειδικοί ανησυχούν ότι η εμπορευματοποίηση των γονιδιακών θεραπειών μπορεί να αδικήσει τους λαούς που, κατά μέσο όρο, έχουν χαμηλότερα εισοδήματα και πιο περιορισμένη πρόσβαση στην υγειονομική περίθαλψη. Για αυτό η Αμερικανική Εταιρεία Γονιδιακής και Κυτταρικής Θεραπείας έθεσε ως κορυφαία προτεραιότητα την εξισορρόπηση των όρων ανταγωνισμού και τη δίκαιη πρόσβαση στις γονιδιακές θεραπείες παγκοσμίως, τονίζοντας την ανάγκη για μια ατζέντα δικαιοσύνης ώστε διασφαλιστεί ότι όλοι μπορούν να ωφεληθούν από αυτή τη τεχνολογία.
from Dnews: Τελευταία νέα και ειδήσεις https://ift.tt/mq98Kvc
via IFTTT

